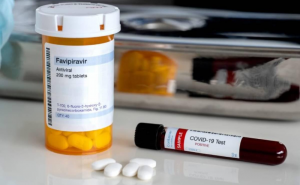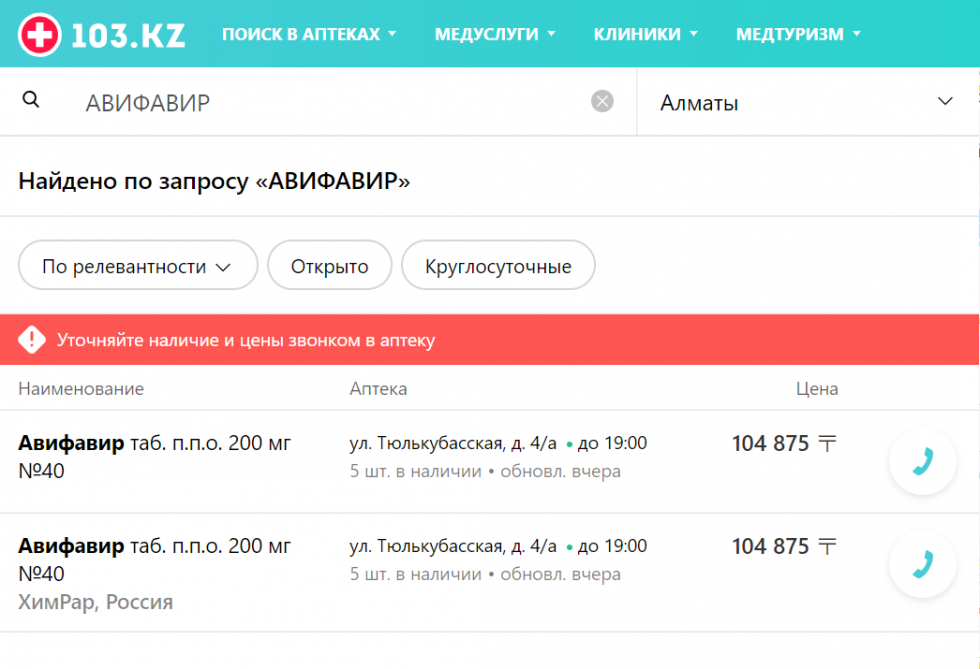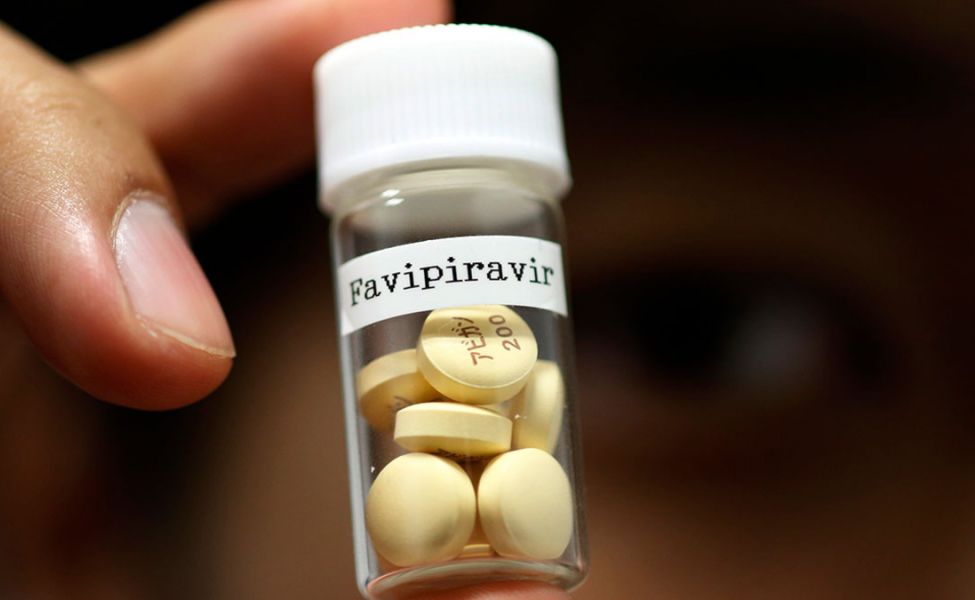
При себестоимости 4,15 тенге российские препараты фавипиравира продаются по цене от 2 до 3 тыс. тенге за таблетку. Полный курс - 100 таблеток
18 июля мы опубликовали пост нейрохирурга Чингиза ШАШКИНА "Доктор Шашкин: Не ведитесь на рекомендации "купленных" врачей!". Вскоре нам написали производители препаратов на основе фавипиравира из Российского фонда прямых инвестиций с просьбой опубликовать их точку зрения в качестве опровержения мнения казахстанского ученого. Ознакомившись с точкой зрения россиян, доктор Шашкин вновь опубликовал пост, в котором уже подробно, со ссылками на первоисточники, рассказал об этом лекарстве.
Здравствуйте, друзья!
На днях мне прислали опровержение на мой пост, который касался применения фавипиравира в лечении коронавирусной инфекции (КВИ).
Суть поста была такова - фавипиравир, противовирусный препарат, который был разработан для лечения совсем другой инфекции, не показал свою эффективность в лечении новой напасти под названием COVID-19 (та же КВИ), а также имеет побочные эффекты, из-за которых он не получил широкого распространения в клинической практике. Поэтому он не имеет права применяться в лечении КВИ, тем более в амбулаторной практике, что активно продвигалось некоторыми отечественными специалистами.
Так вот, российская компания-производитель препарата "Авифавир", содержащий фавипиравир, выступила с опровержением, утверждая, что их препарат, цитирую "первый в России препарат, одобренный для применения против коронавируса, и один из первых зарегистрированных в мире в показании для лечения COVID-19". Но самые главные утверждения были следующие:
- Данные клинических исследований в России, Японии, Китае не были опровергнуты никем из ученых и являются доказанными и статистически достоверными. В результате 3 независимых клинических исследований в России, фавипиравир получил временное регистрационное удостоверение в рамках Постановления Правительства РФ от 3 апреля 2020 г. № 441 и разрешен к повсеместному использованию в российских клиниках.
- Эффективность препарата была официально подтверждена представителями министерства науки и технологий КНР. Препарат фавипиравир официально одобрен к применению в Турции и Индии.
- Препарат успешно использовался для лечения 30 тысяч пациентов из России. Результаты применения фавипиравира показывают, что он сокращает время выздоровления с 9 до 4 дней и облегчает протекание болезни, в том числе снижает высокую температуру".
К дополнению к этому, приведены отзывы некоторых российских врачей, в которых они описывают свой опыт и называют препарат "достаточно эффективным".
Хочу заметить, что опровержение не было подписано кем-то конкретно, а поступило от Внешней пресс-службы РФПИ.
Хорошо, подумал я, давайте разбираться.
Во-первых, по качеству опровержения, я понял, что его писали не медицинские специалисты, а действительно, пресс-служба.
Посудите сами: отсутствие прямых ссылок на клинические исследования, а ссылка на новостной сайт Xinhua, указывает на научно-популярный подход к доказательствам вышеприведенных высказываний.
Для любого уважающего себя Врача, информация из СМИ - это просто вброс, а актуальную информацию ищи на на UpToDate и pubmed.
Также меня смутил разброс приведённых данных: то они пишут о 30000 (тридцати тысячах) успешно пролеченных пациентов. Однако следом уже указано, что исследования проводились в 35 медицинских центрах на 330 пациентах с КВИ. Давайте уже определимся, сколько пациентов было пролечено этим препаратом.
Авторы ссылаются на Постановление правительства РФ от 3 апреля 2020 г. № 441, в рамках которого фавипиравир получил временное регистрационное удостоверение. Сперва я подумал не заморачиваться на чтение юридического документа другой страны, так как это совершенно не касается Казахстана, но все же решил ознакомится с этим интересным документом.
Так вот, согласно вышеуказанному Постановлению, при чрезвычайной ситуации Минздрав выдает разрешение на временное обращение до 1 января 2021 г. серии (партии) лекарственного препарата, незарегистрированного в Российской Федерации и разрешенного для медицинского применения на территории иностранных государств уполномоченными органами соответствующих иностранных государств. Министерство ведет реестр выданных разрешений на временное обращение, который размещается на его официальном сайте в информационно-телекоммуникационной сети Интернет с соблюдением ограничений, установленных законодательством Российской Федерации о персональных данных, коммерческой и (или) государственной тайне, что мы и увидели на соотвествующие сайте. На сайте Госреестра лекарственных средств РФ можно увидеть три препарата фавипиравира (коронавир, авифливир и авифавир), которые получили временную регистрацию до 1 января 2021.
Также, согласно Постановлению "Применение лекарственных препаратов в период чрезвычайной ситуации по показаниям, не указанным в инструкциях по медицинскому применению, с целью изучения их эффективности для проведения профилактических и лечебных мероприятий (далее - применение лекарственных препаратов) вправе осуществлять медицинские и иные организации, которые имеют лицензию на осуществление медицинской деятельности, включены в перечни, утвержденные федеральными органами исполнительной власти и органами государственной власти субъектов Российской Федерации в сфере охраны здоровья в соответствии с их подведомственностью, и в которых планируется и (или) осуществляется медицинская деятельность, направленная на оказание медицинской помощи в условиях чрезвычайной ситуации", - конец цитаты. Таким образом, утверждение пресс-службы РФПИ что препарат "разрешен к повсеместному использованию в российских клиниках" уже является мягко говоря некорректным.
Также в Постановлении указано, что применение лекарственного препарата (получившее временное регистрационное удостоверение - примечание автора), осуществляется на основании решения врачебной комиссии медицинской организации, оформленного протоколом, с внесением информации об этом в медицинскую документацию пациента.
Применение лекарственного препарата возможно также на основании консилиума врачей с внесением решения консилиума в протокол, который подписывается участниками консилиума врачей, и с указанием соответствующей информации в медицинской документации пациента. При начале применения лекарственного препарата ответственное лицо медицинской организации представляет в министерство и Федеральную службу по надзору в сфере здравоохранения в форме электронного документа информацию, содержащую даты начала и окончания применения лекарственного препарата, наименование лекарственного препарата, название заболевания (состояния) по международной классификации болезней, для профилактики и (или) лечения которого применяется лекарственный препарат, с приложением к этой информации копии инструкции по медицинскому применению такого лекарственного препарата.
То есть, обратите внимание, какие серьезные и важные меры предосторожности применяются, согласно российскому законодательству, при обращении таких препаратов! Это значит, что применение препарата фавипиравир возможно ТОЛЬКО В СТАЦИОНАРНЫХ УСЛОВИЯХ и только в рамках клинических исследований! Практически невозможно осуществить такие меры в амбулаторных условиях.
Идём далее! В Постановлении указано, что "Изучение эффективности применения лекарственных препаратов осуществляется в рамках малоинтервенционного исследования с соблюдением принципов надлежащей клинической практики в соответствии с протоколом (программой) научного исследования, утверждаемым независимым этическим комитетом, созданным организацией.
Результаты научного исследования эффективности применения лекарственных препаратов используются для формирования клинических рекомендаций, а также могут служить основанием для внесения разработчиком лекарственного препарата изменений в инструкцию по медицинскому применению лекарственного препарата.
Организация в течение 10 дней после завершения применения лекарственного препарата направляет в министерство в форме электронного документа отчет о результатах применения лекарственного препарата с соблюдением ограничений, установленных законодательством Российской Федерации в области персональных данных".
Из вышеуказанного следует полагать, что те указанные в опровержении 35 медицинских центра, входят в "перечни, утвержденные федеральными органами исполнительной власти и органами государственной власти субъектов Российской Федерации в сфере охраны здоровья в соответствии с их подведомственностью, и в которых планируется и (или) осуществляется медицинская деятельность, направленная на оказание медицинской помощи в условиях чрезвычайной ситуации", во всех утверждены протоколы исследований и утверждены независимыми этическими комитетами. Во всех случаях клинических исследований результаты уже были отправлены в уполномоченный орган, и по ним были вынесены соответствующие решения. Я уже не буду описывать процедуру установления предельных цен и мониторинг дефектуры, либо отсутствия в обращении, которые проводятся при регистрации.
Таким образом, следует вывод, что на основании предоставленных данных и данных из открытых источников, российский аналог фавипиравира проходит клинические исследования в РФ сроком до 1 января 2021 года.
Этот факт не даёт оснований утверждать, что Авифавир разрешён к повсеместному клиническому использованию на территории Российской Федерации. Право работы с препаратом имеют только некоторые клиники, включённые в федеральные перечни. В свободном информационном пространстве не обнаружены доступные клинические протоколы, по которым проводятся исследования, а также результаты применения препарата. Следует понимать, что клинические исследования ещё продолжаются, т.к. это длительный процесс и требует:
1) четкого анализа данных;
2) наличия соответствующих ресурсов;
3) публикаций в открытых научных медицинских изданиях.
На последний пункт я бы обратил отдельное внимание. Согласно рекомендациям и правилам научного сообщества (и не только медицинского), результаты любых исследований должны быть рецензированы соответствующими специалистами, опубликованы в открытых источниках, после чего они становятся достоянием так называемой доказательной медицины. Это тогда, когда источнику, исследователям можно доверять, а результаты можно использовать для применения в практике.
То есть, доказательная медицина - это поверенная и качественная информация. Все, что иное - это не то. Даже выступление крупного китайского чиновника во всемирно известном новостном ресурсе Xinhua не является доказательной медициной. Это - новость, а новости бывают разные. Например такая: Фавипиравир оказался неэффективен при лечении коронавирусной инфекции.
Но это опять-таки новость, а не источник!
Самый главный и достоверный источник информации для практикующих врачей мира - это англоязычный ресурс UpToDate.
Согласно этому источнику, фавипиравир не зарегистрирован в США, находится в стадии исследования по применению для лечения КВИ, и в настоящее время его безопасность и эффективность не определены. Определены дозы лекарства для лечения КВИ и используются только в исследовательских целях.
В источнике описаны побочные эффекты фавипиравира на примере препарата Авиган (Япония): гастроинтестинальные (тошнота, рвота, снижение аппетита, диарея), эндокринные и метаболические - повышение уровня мочевой кислоты, гематологические - снижение уровня нейтрофилов и повреждение печени. Препарат абсолютно противопоказан для беременных и кормящих женщин. Стоимость одной таблетки составляет 0,01 долларов США - по сегодняшнему курсу - 4,15 тенге (в Казахстане препараты на основе фавипиравира продаются по цене от 2 до 3 тыс. тенге за таблетку, на курс лечения требуется 100 таблеток - Ред.)
Несомненно, такие же исследования безопасности и эффективности фавипиравира российского происхождения должны быть проведены до массового использования в практике.
Следующий важный источник - это Промежуточное руководство "Clinical Management of COVID-19" от 27 мая 2030 года, разработанное ВОЗ, в котором четко написано, что ряд лекарственных препаратов, в том числе фавипиравир, не применяются для лечения и профилактики КВИ, если только не для клинических исследований.
Согласно открытому ресурсу clinicaltrials.gov, в настоящее время из более чем 2000 клинических исследований по лечению КВИ в мире проводится шесть клинических исследований по применению фавипиравира в лечении КВИ из следующих стран: Италия, Саудовская Аравия, Россия, Великобритания, Турция и Египет. В ресурсе clinicaltrialsarena.com есть информация ещё об одном клиническом исследовании группы из Индии, которое завершится в июле-августе этого года.
Из шести исследований ещё ни по одному не получено результатов. В числе исследований есть и российское под названием An Adaptive Study of Favipiravir Compared to Standard of Care in Hospitalized Patients With COVID-19, которое проводится в нескольких центрах на 330 стационарных пациентах. Скорее всего это те пациенты, о которых упоминалось в опровержении. В статусе исследования закреплено Active, not recruiting, что означает, что исследование идёт, участники получают лечение и оцениваются, но потенциальные участники исследования в настоящее время ещё не рекрутированы и не вовлечены в исследование. Дата окончания исследования указана - июль 2020 года, т.е. дата, когда последний пациент получит лечение и будет оценён. Таким образом, на сегодняшний день, 28 июля, исследование завершается. Результатов на сайте ещё нет. В доступном сервисе pubmed результатов этого исследования не найдено.
Заслуживает внимания клиническое исследование Early Intervention in COVID-19: Favipiravir Verses Standard Care (PIONEER), которое инициировано Chelsea and Westminster NHS Foundation Trust в сотрудничестве с японской компанией FUJIFILM Tanaka Chemical Co и другими коллабораторами.
Исследование включит 450 участников и завершится 31 марта 2021 года. Интересно, для чего японским производителям Авигана (фавипиравира) нужно проводить его большое клиническое исследование, если его эффективность, как утверждают мои оппоненты, уже доказана и не вызывает сомнений?
Таким образом, исследование фавипиравира его же производителем ещё продолжается.
На научном ресурсе researchgate.net опубликована статья Experimental Treatment with Favipiravir for COVID-19: An Open-Label Control Study, в которой китайские ученые сравнили эффективность в лечении КВИ фавипиравира и другого противовирусного препарата лопинавир/ритоновир. Результаты показали лучший эффект от фавипиравира. Похожее исследование было проведено в сравнении с арбидолом. Наверное, не нужно говорить, что к нашей теме эти исследования не имеют никакого отношения, т.к. не имеют сравнения со стандартной терапией.
Таким образом, можно сделать вывод, что в настоящее время идут научные исследования, в том числе и в России, но убедительных данных, даже предварительных, о безопасности и эффективности применения фавипиравира у пациентов с COVID-19 пока нет.
Все клинические исследования проводятся в стационарных условиях по строго разработанному протоколу, поэтому об амбулаторном применении фавипиравира говорить нельзя.
Таким образом, утверждение, что эффективность фавипиравира доказана в клинических исследованиях, является преждевременным.
Хочется надеятся, что фавипиравир всё-таки покажет свою эффективность для лечения КВИ, тогда мы получим хорошее лекарство. Но пока применять его рано и тем более в амбулаторной практике!
Всем добра и здоровья!
Ссылки по теме:
Favipiravir shows good clinical efficacy in treating COVID-19: official
Фавипиравир оказался неэффективен при лечении коронавирусной инфекции
Источник: страница Чингиза Шашкина в Facebook. Публикуется с разрешения автора.
Фото: Issei Kato / Reuters.